|
iiiiiiiii | Avril – Mai 2018 |
| iiiiiiiii |  |
|
|
|
||
|
|
||
 |
– Dans le numéro 234 de Spectra Biologie –
Consultez gratuitement nos vidéos et interviews !
Témoignages-client (sponsorisés)
 |
Innovations |
Système d’hémostase automatisé multiparamétrique
S’inscrivant dans la lignée reconnue des systèmes de la génération Max, le nouvel automate d’hémostase multiparamétrique de Stago, le STA Compact Max 3, présente de nouvelles fonctionnalités significatives et attendues.
Son module EPC – Expert Preanalytical Check – permet un réel contrôle du volume de remplissage ainsi qu’une détection des échantillons hémolysés, ictériques ou lipémiques (HIL) directement au niveau de l’aiguille sans consommation de plasma, ni incidence sur la cadence. Ce nouveau module vient renforcer la fiabilité de son système de détection viscosimétrique (VBDS), technologie chronométrique exclusive standardisée et éprouvée sur l’ensemble de la gamme.
Dans sa classe d’analyseurs, le STA Compact Max 3 optimise encore sa productivité en minimisant ses opérations de maintenance manuelles et en améliorant son ergonomie par des évolutions technologiques du système de pipetage : nouveau module PSR (Pipette Simple Résolution) et nouvelle aiguille pour le cap piercing.
Des évolutions logicielles apportent un vrai management de l’urgence (STAT) pour optimiser le TAT (Temps d’Analyse Total / Turn Around Time) et améliorer la traçabilité. L’expertise de l’analyseur est renforcée pour une parfaite gestion des règles de ré-analyses (reflex testing) basées sur des algorithmes cliniques renouvelés. Le contrôle de la qualité est aussi concerné par ces évolutions avec une plateforme web de CQI externalisé, My Expert QC, connectable à l’analyseur.
Une gamme complète de solutions dédiées à l’hémostase
Horiba Medical a développé une nouvelle gamme d’analyseurs et de réactifs dédiés à l’hémostase : la gamme Yumizen G.
En élargissant son domaine d’activité à une discipline complémentaire de l’hématologie, la société est désormais en mesure de proposer à ses clients une solution dédiée et spécifique à chaque laboratoire.
La gamme Yumizen G est conçue pour répondre aux besoins des différents laboratoires :
– Yumizen G100 INR, le plus petit analyseur de la gamme, est conçu pour la détection de l’INR en laboratoires satellites ou en biologie délocalisée.
– Yumizen G200 et Yumizen G400, analyseurs semi-automatiques compacts (2 ou 4 canaux respectivement), sont dédiés aux petits laboratoires pour les tests de dépistage en hémostase et les D-dimères.
– Yumizen G800, analyseur de paillasse compact, s’adresse aux laboratoires de moyenne activité.
– Yumizen G1550, analyseur haute capacité entièrement automatisé, peut répondre aux attentes des laboratoires de moyenne et forte activité.
Cette offre globale est associée à la gamme de réactifs Horiba Medical pour les tests de routine et spécifiques, développée et optimisée pour les analyseurs Yumizen G.
Nouvelle solution de typage microbien
Bruker a annoncé le lancement lors du dernier congrès de l’ASM 2017 à la Nouvelle-Orléans (Etats-Unis), de sa nouvelle plateforme nommée IR Biotyper® pour le typage d’espèces microbiennes, en quelques heures seulement.
Cette nouvelle technique de typage rapide, facile d’utilisation et économique, répond clairement à des besoins exprimés par les équipes d’hygiène hospitalière, afin de gérer et de contrôler les infections, d’étudier les phénomènes épidémiologiques et de comprendre la pathogénicité des infections quasiment en temps réel.
Selon Bruker, cette solution de spectrométrie Infra-Rouge présente un pouvoir de discrimination comparable à celui des techniques de biologie moléculaire traditionnellement utilisées dans ce domaine.
Dans un flux de travail commun, cette plateforme est le complément optimal de la solution MALDI Biotyper® déjà très fortement implémentée au sein des laboratoires de microbiologie, en alliant la précision et la rapidité d’identification d’un microorganisme via le MALDI-TOF.
Automate de diagnostic moléculaire tout-en-un
Le partenariat entre Randox Laboratories, un des leaders du diagnostic in vitro au Royaume-Uni, et le géant allemand Bosch a abouti au lancement d’une nouvelle plateforme de diagnostic moléculaire : Vivalytic.
Ce système réunit la plus large gamme de tests pour un appareil de cette taille. Utilisant la technologie Biochip Array brevetée par Randox, cette plateforme PCR multiplexe est très facile à utiliser et très complète. Selon l’application de test, les résultats seront délivrés à partir de 30 minutes.
Les tests moléculaires de Randox continuant à être développés, le portefeuille de tests potentiels sur cette plateforme universelle n’est pas limité, et ses résultats sont rapides et précis. Les premiers tests disponibles sur le système sont les panels de Randox pour les infections respiratoires et les infections sexuellement transmissibles (IST), déjà marqués CE.
Le kit multiplexe pour le système respiratoire détecte simultanément 22 pathogènes viraux et bactériens, y compris Bordetella parapertussis – sans avoir besoin de tests secondaires ou de confirmation.
Le kit STI permet la détection de 10 IST virales, bactériennes et protozoaires à partir d’un seul échantillon d’urine ou d’un écouvillon urogénital. Chlamydia trachomatis, N. gonorrhoeae, Trichomonas vaginalis et Treponema pallidum, qui peuvent tous être détectés sur la biopuce, sont parmi les causes les plus fréquentes. Identifier ces infections correctement la première fois réduit la mauvaise utilisation des antibiotiques et soutient leur utilisation ciblée. Il améliore les résultats pour les patients et réduit les coûts associés à la détection d’une seule infection.
Le Dr FitzGerald, des laboratoires Randox, a déclaré : « C’est un partenariat idéal pour Randox, combinant notre expertise dans le diagnostic de laboratoire moléculaire avec l’ingénierie de pointe de Bosch. Avec la résistance aux antibiotiques, l’un des problèmes de santé publique les plus urgents auxquels nous soyons confrontés mondialement, nous sommes ravis que les premiers tests disponibles sur Vivalytic soient nos meilleurs panels multiplex pour les infections respiratoires et sexuellement transmissibles. »
Vivalytic et ses panels ont été présentés aux professionnels pour la première fois au Congrès ECCMID en avril 2018, à Madrid.
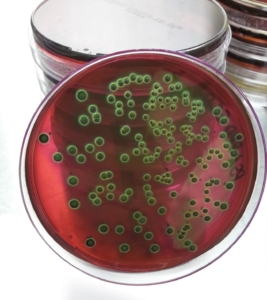
Gamme complète pour la détection des résistances aux polymyxines
Ces dernières années, les bactéries résistantes aux antibiotiques, et parmi elles les entérobactéries productrices de carbapénémases (EPC), ont pris une importance clinique de plus en plus significative. Néanmoins, les EPC restent habituellement sensibles aux polymyxines (Colistine et Polymyxine B), des antibiotiques dits d’ancienne génération mais dont l’intérêt thérapeutique a été récemment redémontré.
Dans ce contexte, ELITech Microbio a développé une gamme complète de tests permettant de détecter en à peine 2–3 heures les souches sensibles ou résistantes à la colistine. Les tests Rapid Polymyxin™ NP (entérobactéries), Rapid Polymyxin™ Pseudomonas et Rapid Polymyxin™ Acinetobacter, permettent de détecter les sensibilités et résistances des entérobactéries, P. aeruginosa et A. baumannii vis-à-vis des polymyxines à partir d’une culture bactérienne sur milieu gélosé. Dans le cas des entérobactéries, la recherche de résistance est également possible en 3–4h directement depuis une hémoculture positive.
En parallèle, ELITech Microbio a lancé la SuperPolymyxin™, gélose sélective permettant la détection des bactéries gram négatif présentant des résistances acquises ou intrinsèques à la colistine. Cette gélose permet ainsi une mise en place immédiate d’une antibiothérapie appropriée, ou l’identification de sujets porteurs de souches résistantes à la colistine (suivi d’une confirmation de la résistance par un des tests de la gamme Rapid Polymyxin™) afin de limiter les risques de diffusion épidémique.
Tube de prélèvement sanguin d’ADN acellulaire circulant pour les cancers et DPNI
Becton Dickinson a annoncé la mise sur le marché du tube Blood ccfDNA, marqué CE-IVD, de PAXgene®. Ce tube de prélèvement en plastique qui contient un additif breveté de stabilisation de l’échantillon et une technologie BD Vacutainer® Hemogard™ pour aider à protéger la sécurité des travailleurs de la santé, a été conçu pour assurer des résultats précis et reproductibles dans les applications de tests de diagnostic moléculaire utilisant de l’ADN acellulaire circulant (ccfDNA), tels que les tests du cancer et prénataux non invasifs. Le produit a été développé par PreAnalytiX GmbH, une joint-venture entre BD et Qiagen.
Les tests de diagnostic moléculaire utilisant l’ADN acellulaire circulant permettent d’éviter le recours aux biopsies tissulaires ou aux tests similaires invasifs. Le tube Blood ccfDNA de PAXgene fournit une solution pour permettre aux laboratoires de stabiliser les échantillons lorsqu’ils ne peuvent pas être traités le jour même du prélèvement. Alors que les tubes EDTA standards nécessitent un traitement dans les quelques heures avant que les cellules ne meurent et libèrent l’ADN génomique dans le plasma sanguin (modifiant ainsi le profil de l’ADN acellulaire natif circulant), ce nouveau tube contient un agent chimique de stabilisation unique qui permet le prélèvement et le traitement à des jours différents, surmontant un obstacle logistique majeur pour les laboratoires de référence proposant des analyses moléculaires en-dehors du cadre hospitalier.
« De nombreux laboratoires de diagnostic moléculaire, en particulier dans la sphère du cancer, développent de nouveaux tests pour la surveillance et le dépistage des patients. Ils ont besoin d’un système sûr, cliniquement acceptable, pour le prélèvement du sang et le traitement de l’ADN acellulaire circulant qui est capable de stabiliser un échantillon de manière à ce que l’extraction de l’ADN acellulaire circulant puisse être réalisée après que l’échantillon ait été transféré en un autre lieu, chose qui est impossible avec les tubes EDTA » souligne Frank Augello, directeur général, PreAnalytiX GmbH.
 |
Actualités |
L’intelligence artificielle de Sophia Genetics s’apprête à révolutionner le diagnostic
Le premier test génomique clinique au monde marqué CE-IVD
Sophia Genetics, spécialiste mondial de la médecine basée sur les données, est la première société au monde à avoir reçu le marquage CE-IVD pour son test génomique clinique par capture d’hybrides. L’application de diagnostic moléculaire standardisée représente une avancée majeure dans le diagnostic des troubles hématologiques. Cela inclut des maladies telles que la leucémie, qui représente 2,5 % des cancers dans le monde et 30 % des cancers chez les enfants et les adolescents. Ce test couvre les gènes associés aux troubles hématologiques et fournit aux cliniciens une solution complète pour l’identification rapide et précise des mutations de l’ADN de leurs patients.
L’application de diagnostic moléculaire « Myeloid Solution by Sophia Genetics » garantit des performances analytiques et cliniques supérieures dans la détection des mutations génomiques responsables des syndromes myélodysplasiques (SMD), des néoplasmes myéloprolifératifs (NMP) et des leucémies. Elle garantit un pourcentage élevé de lectures de séquences et une couverture exceptionnelle dans les régions riches en GC, y compris le premier exon. Les limitations techniques liées à l’analyse des biomarqueurs clés tels que CEBPA, FLT3 et CALR sont surmontées grâce à cette solution standardisée.
Cette application représente un progrès majeur dans la personnalisation des parcours de soin des patients atteints d’un cancer. Ceci facilitera l’accès des patients, dans le monde entier, à une solution de diagnostic clinique, qui permettra d’identifier le traitement le plus approprié en fonction de l’empreinte moléculaire du cancer de chaque individu. L’industrie pharmaceutique pourrait par conséquent optimiser le développement des médicaments axés sur les biomarqueurs et offrir à chaque patient le traitement le plus adapté.
Malgré une baisse des taux de mortalité associés aux troubles hématologiques, le nombre de nouveaux cas diagnostiqués augmente. Cette nouvelle application réduit la complexité et le délai du diagnostic clinique grâce à une solution standardisée et facilement accessible, permettant aux cliniciens de diagnostiquer plus précisément les patients atteints de troubles hématologiques.
Démocratiser la médecine basée sur les données
Elaborées grâce à l’intelligence artificielle (IA), les solutions de cette société résolvent les problèmes liés à la complexité d’analyse des données génomiques en détectant de manière très précise, les mutations de l’ADN qui cause des maladies comme le cancer. En mai, l’IA SOPHiA avait déjà été déployée dans plus de 450 hôpitaux dans 60 pays et avait aidé à mieux diagnostiquer plus de 208 000 patients. Le nombre de patients atteint maintenant les 10 000 par mois.
Le réseau constitué par tous ses partenaires (hôpitaux, institutions, entreprises telles que Roche ou Novartis) constitue la plus grande communauté de génomique clinique au monde. Les données récoltées ne se limitent pas au génome mais explorent également d’autres aspects (étalonnage des traitements, évaluation des protocoles médicaux…) pour affiner les analyses. Via leur plateforme, le médecin peut rechercher les caractéristiques moléculaires spécifiques à une tumeur ou à une maladie congénitale pour proposer le traitement le plus pertinent.
Selon son fondateur Jurgi Camblong, docteur en biologie moléculaire français qui veut démocratiser la médecine basée sur les données, la plupart des cancers pourraient être maîtrisés dans 10 ans.
La start-up suisse Sophia Genetics a été classée 30e parmi les 50 compagnies les plus intelligentes par le MIT Tech Review, et classée 5e parmi les 10 biotech les plus innovantes au monde selon le prestigieux classement du magazine américain Fast Company.
Basée près de l’université de Lausanne, la société a annoncé l’installation de son centre de R&D à Bidart, au pays basque. Après avoir réussi 2 levées de fonds à 30 millions de dollars chacune, l’entreprise, qui comptait 20 salariés en 2014, espère réunir plus de 200 employés d’ici fin 2018 et prépare son entrée en bourse qu’elle prévoit pour la fin de l’année 2019.
bioMérieux acquiert Astute Medical et renforce son offre en immunoessais
Cette acquisition fait suite au partenariat conclu en 2015 entre les deux sociétés, lorsqu’Astute a accordé à bioMérieux une licence pour le développement et la commercialisation du test Nephrocheck® pour le système d’immunoessais automatisés Vidas®. En outre, bioMérieux distribue depuis 2017 ce test sur le système Astute140 Meter aux États-Unis.
Astute Medical a constitué un solide réseau de leaders d’opinion et a démontré la forte valeur du test Nephrocheck® sur la base d’études d’impact sur la santé des patients revues par des pairs. bioMérieux prévoit de continuer à investir dans de telles études médico-économiques, d’explorer le potentiel d’autres biomarqueurs prometteurs du pipeline d’innovation d’Astute et de travailler avec les partenaires de ce dernier disposant actuellement d’accords de licence et de distribution afin de rendre ce test phare disponible sur le plus grand nombre possible de marchés.
L’IRA est un enjeu majeur de santé publique : c’est une maladie fréquente, coûteuse et potentiellement mortelle pour les patients hospitalisés. Aujourd’hui, jusqu’à 50 % des patients en soins intensifs développent une IRA. Cela peut allonger la durée des séjours à l’hôpital, évoluer en insuffisance rénale chronique, accroître le risque de mortalité et augmenter les coûts de prise en charge. Une récente étude fait état d’une baisse de 33,9 % des cas d’IRA modérée à sévère à la suite d’une intervention de chirurgie cardiaque, lorsque les cliniciens utilisent le test Nephrocheck® pour identifier les patients présentant un risque d’IRA modérée à sévère puis mettent en œuvre un ensemble de soins suivant les recommandations de la Foundation Kidney Disease Improving
Global Outcomes (KDIGO).
« De par sa pertinence dans de nombreuses pathologies sévères, le test Nephrocheck® développé par Astute s’inscrit parfaitement dans la stratégie de bioMérieux visant à différencier le système d’immunoessais Vidas® par des marqueurs brevetés ainsi qu’à fournir à nos clients des solutions diagnostiques innovantes et à forte valeur médicale pour une meilleure prise en charge des patients » a déclaré Alexandre Mérieux, Président Directeur Général.
Qiagen pénètre le marché des tests multiplexes syndromiques grâce à Stat-Dx
Comme la société l’avait prévu en janvier, Qiagen a finalisé au second trimestre le rachat de Stat-Dx, une société privée développant une plateforme multiplexe de tests moléculaires élaborés selon l’approche syndromique. Basé sur la technologie de PCR en temps réel, ce système permet, à partir des symptômes du patient, de tester simultanément les principaux agents pathogènes potentiellement responsables ou plusieurs cancers et ainsi d’éviter des successions d’analyse onéreuses et retardant la prise en charge. QIAstat-Dx est maintenant lancée avec un panel respiratoire amélioré marqué CE-IVD qui détecte 21 pathogènes ; le système dispose déjà d’une base installée importante parmi les premiers utilisateurs.
La plateforme, baptisée QIAstat-Dx, permet de tester jusqu’à 48 cibles moléculaires simultanément, pour le diagnostic de syndromes tels que des infections respiratoires ou gastro-intestinales graves, ou pour une utilisation en oncologie. Les tests sont annoncés comme étant plus économiques, faciles à utiliser et adaptables à tout type d’échantillon clinique :
le système pourra fournir des renseignements qualitatifs et quantitatifs en une heure environ sur la cause précise des divers syndromes. Qiagen souhaite que ce système puisse contribuer à une plus grande diffusion des tests moléculaires.
Basé sur la technologie propriétaire DiagCORE®, la plateforme avait été dévoilée en avril 2017 au Congrès Européen de Microbiologie Clinique (ECCMID) et a reçu un premier marquage CE-IVD en janvier 2018. Un panel des infections gastro-intestinales va également être lancé en Europe au second semestre 2018, aux Etats-Unis en 2019 puis sur d’autres marchés internationaux en fonction des délais réglementaires respectifs. Des tests supplémentaires sont en cours de développement, et portent sur les maladies infectieuses, la surveillance de la réponse immunitaire, l’oncologie et les diagnostics compagnons.
Un rachat stratégique
La demande de diagnostic moléculaire par l’approche syndromique augmente rapidement. Pour les syndromes respiratoires et les tests de la grippe, Qiagen estime le marché total potentiel à environ 1,5 million de tests par an aux États-Unis et à 1,1 million en Europe. Pour les syndromes gastro-intestinaux, le nombre de cultures ou autres méthodes actuellement utilisées est estimé à 2,6 millions par an aux Etats-Unis et à environ deux millions en Europe, avec un nombre relativement faible mais en croissance rapide de tests utilisant des diagnostics moléculaires.
D’autre part, mieux identifier les pathogènes avant de choisir la thérapeutique constitue un atout supplémentaire dans la lutte contre les résistances bactériennes aux antibiotiques en permettant de mieux cibler les traitements.
Qiagen, qui souhaite emprunter ce nouveau segment de marché porteur et innovant, a choisi d’intégrer à ses activités la société barcelonaise Stat-Dx, fondée en 2010, pour environ 147 millions de dollars en espèces au départ, auxquels s’ajoutent des paiements additionnels à concurrence de 44 millions de dollars en fonction des étapes réglementaires et commerciales. L’acquisition devrait être financée par des réserves de trésorerie existantes. Pour 2018, environ 7 millions de dollars de ventes sont attendus suite au lancement de QIAstat-Dx en Europe et sur d’autres marchés, tandis que des ventes d’au moins 30 millions de dollars sont prévues en 2019.
Diaxonhit fusionne ses deux filiales Eurobio et InGen
Le 4 avril 2018, Diaxonhit, groupe français leader dans le diagnostic médical in vitro et les sciences de la vie, annonçait la fusion de ses deux filiales, Eurobio et InGen, en une entité unique, eurobio-ingen basé aux Ulis. Au-delà d’une simplification structurelle, l’objectif de cette fusion est de finaliser juridiquement la mise en œuvre des synergies liées à l’acquisition d’Eurobio en mars 2017 afin de créer un acteur majeur du diagnostic et des sciences de la vie en France.
2017 : une année de rupture pour Diaxonhit
A la suite d’une première acquisition en 2012, celle d’InGen, Diaxonhit devenait le premier distributeur indépendant de produits de diagnostic in vitro (« DIV ») sur le marché français. Toutefois cette acquisition ne lui a pas permis de renforcer suffisamment son portefeuille de produits propriétaires ni d’atteindre l’équilibre financier.
Fin mars 2017, l’entreprise a réalisé une deuxième acquisition majeure, celle d’Eurobio pour un montant total de 28,9 millions d’euros. Le nouveau groupe ainsi constitué a atteint une taille critique sur le marché du DIV et celui des sciences de la vie avec une présence élargie à des marchés complémentaires et en croissance, un portefeuille accru de produits propriétaires innovants, une force de vente importante, et de nombreux leviers de croissance, notamment par le développement à l’international. Cette acquisition, combinée à des mesures d’économie et de réorganisation – transfert du siège de Diaxonhit vers les locaux d’Eurobio aux Ulis, unification des deux équipes, entre autres – avait également pour objectif d’amener rapidement le groupe à l’équilibre financier.
Grâce à la mise en œuvre rapide des synergies liées à l’acquisition, Diaxonhit a pu procéder dès le début 2018 à une simplification du groupe en fusionnant ses filiales InGen et Eurobio. La nouvelle entité nommée eurobio-ingen, dont le siège est désormais aux Ulis avec celui de Diaxonhit, dispose de deux établissements situés aux Ulis (production) et à Chilly-Mazarin (commercial et administration). Elle emploie un total de 99 collaborateurs.
2018 : développement d’un acteur majeur en France
Ainsi, eurobio-ingen devient un acteur majeur du diagnostic et des sciences de la vie en France ; en témoigne la forte progression de 9 % de son chiffre d’affaires pro forma entre 2016 et 2017 quand l’ensemble du secteur était en faible croissance.
Son activité s’étend de la conception au développement et à la commercialisation de réactifs de laboratoire dédiés au domaine des sciences de la vie, ainsi que des tests de diagnostic in vitro dans les domaines de la transplantation, des maladies infectieuses, de l’auto-immunité et de l’oncologie.
Avec ses nombreux partenariats et sa forte présence hospitalière, eurobio-ingen dispose de son propre réseau étendu de commercialisation et d’un portefeuille de produits propriétaires parmi lesquels les tests de diagnostic Tétanos Quick Stick®, et la gamme de biologie moléculaire EurobioPlex (Dengue, Chickungunya, Zika, Hépatite
Delta, etc…) dans le domaine des maladies infectieuses.
Dans le domaine des sciences de la vie, eurobio-ingen développe et commercialise un ensemble de produits propriétaires, destinés aux centres de recherche (CNRS, Instituts…), en particulier auprès d’organismes publics de recherche, de sociétés de biotechnologie et de l’industrie pharmaceutique : milieux de culture cellulaire, réactifs de biologie moléculaire, anticorps propriétaires, service de production à façon.
Pour l’année 2018, Diaxonhit veut continuer son développement, notamment grâce à la gamme de diagnostic Eurobioplex en biologie moléculaire et à de nouveaux accords de distribution afin de proposer des produits de technologie innovante, comme le NGS (Next Generation Sequencing).
Eurobio-ingen, distributeur exclusif de la plateforme Verigene® de Luminex
Eurobio-ingen, a obtenu du groupe international Luminex®, basé aux Etats-Unis, un accord exclusif de distribution de la gamme de tests de biologie moléculaire Verigene® et des automates associés. Cet accord couvre la France et les pays du Maghreb.
Cette nouvelle offre vient compléter les gammes de biologie moléculaire eurobio-ingen déjà existantes en proposant une solution de diagnostic multiplexée. Luminex est propriétaire de la gamme Verigene depuis 2016 suite à l’acquisition de la société Nanosphere.
La solution Verigene® permet grâce à un panel de PCR multiplexes automatisées sur un système dédié d’identifier spécifiquement les pathogènes impliqués dans les sepsis, les complications respiratoires, ou encore les gastro-entérites virales ou bactériennes.
Particulièrement adapté aux situations d’urgence de jour comme de nuit, le fonctionnement au coup par coup du système fournit une identification précise et rapide du ou des pathogènes responsables de l’infection ainsi que de leurs résistances potentielles aux antibiotiques sans recourir à des méthodes de culture fastidieuses.
Sa facilité d’utilisation intéressera particulièrement les laboratoires hospitaliers disposant de services d’urgence, de réanimation ou encore de soins intensifs.
La mise à disposition de ces informations critiques par le laboratoire donne l’opportunité aux cliniciens d’adapter les soins et d’améliorer la prise en charge des patients.
Le vaccin anti-chlamydia en approche
Le CRI – Centre de Recherche sur l’Inflammation (Paris Diderot/Inserm) – est porteur d’un projet de maturation ambitieux de développement d’un vaccin anti-chlamydia. Financée par la SATT IDF Innov, cette recherche répond à la stratégie mondiale du secteur de la santé portée par l’OMS, qui vise à lutter contre les infections sexuellement transmissibles (IST) et qui appelle à une action immédiate.
131 millions de personnes contractent une infection à chlamydia chaque année dans le monde parmi les 15–49 ans selon l’OMS, et le nombre de cas augmente depuis une quinzaine d’années. Cette IST, « silencieuse » chez la plupart des personnes infectées, reste difficile à diagnostiquer, se propage plus facilement et augmente le risque de co-infection avec d’autres IST, telles que le sida.
Bien que l’infection soit facile à traiter, elle peut entraîner de sérieux problèmes de santé si elle n’est pas décelée et traitée rapidement. L’OMS préconise donc, dans le cadre de son plan de lutte contre les IST 2016–2021, une vaccination préventive pour lutter contre les infections à chlamydia, mais aucun vaccin n’est disponible à ce jour.
Or, au cours de l’été 2013, l’équipe d’IDF Innov rencontre Colette Kanellopoulos-Langevin, directrice de recherche émérite au CNRS, et Philippe Verbeke, maître de conférence à l’université Paris Diderot, tous deux chercheurs au CRI de la faculté de médecine de l’hôpital Bichat à Paris, dirigé par Renato Monteiro.
Les deux chercheurs travaillent alors sur la création d’un vaccin anti-chlamydia sans adjuvant, de conception originale. Classiquement, un vaccin est un produit issu du microbe infectieux pour déclencher une mémoire immunitaire contre ce pathogène. Les chercheurs ont eu l’idée d’utiliser une chlamydia tuée par des antibiotiques pour constituer le vaccin. Cette approche, totalement nouvelle pour le développement d’un vaccin, est une véritable innovation de rupture. IDF Innov a ainsi décidé de soutenir le développement de la technologie via un projet de maturation démarré en 2014.
Les résultats, obtenus récemment, sont particulièrement prometteurs et ont conduit au dépôt d’une demande de brevet. L’équipe a ainsi pu identifier les modes d’action du vaccin, tester plusieurs voies d’administration du traitement, et évaluer la mémoire immunitaire à long terme. De façon surprenante, elle a de plus pu démontrer que l’injection du vaccin après infection entraîne une baisse significative de la charge bactérienne.
Cela ouvre des perspectives très encourageantes pour le développement d’un vaccin sûr et efficace à la fois sur des personnes saines ou déjà infectées.
Une méthode optique innovante pour l’océanologie, bientôt dans les LBM
L’expédition Tara Océans visait à prélever du plancton pour étudier l’effet du réchauffement climatique sur les systèmes planctoniques et coralliens. C’est pour répondre à une demande de biologistes du projet que des chercheurs de l’Institut Langevin se sont mis en quête d’une méthode simple pour caractériser les virus dans des échantillons d’eau de mer. Les méthodes utilisées jusqu’ici recouraient à la microscopie électronique, longue à mettre en œuvre, ou à des techniques d’interférométrie optique délicates à maîtriser. La méthode innovante proposée par l’Institut Langevin est plus facile à utiliser. Comme l’ont montré les essais menés, elle permet de compter et distinguer différentes catégories de virus (de taille comprise entre 20 et 100 nm), mais aussi de détecter des vésicules et de les différencier des virus.
La nouvelle méthode de détection, brevetée, utilise une source lumineuse Led et mesure les interférences entre la lumière diffusée par les particules en suspension et le faisceau de référence qui les illumine. « Contrairement à un interféromètre traditionnel à deux ondes, qui sépare les faisceaux en deux, dans notre instrument les lumières ne passent que par un seul chemin optique. Ce qui le rend insensible aux vibrations ou aux différences de température », explique Claude Boccara. Le dispositif mesure l’amplitude de la lumière diffusée par une nanoparticule, amplitude qui dépend de sa taille. Une caméra rapide (150 à 700 images/seconde) suit les trajectoires du mouvement brownien, qui sont reliées à la taille et à la morphologie des particules (filaments de certains virus…). Ces deux mesures couplées permettent de mesurer et de différencier des virus de différentes tailles et de leur attribuer une signature spécifique.
Pour valoriser ces résultats, les chercheurs se sont associés à Quattrocento, un « company builder » qui développe et industrialise des instruments et des dispositifs médicaux à partir d’inventions nées dans des laboratoires. Les partenaires ont créé en septembre 2017 la start-up Myriade, dont Quattrocento est l’actionnaire majoritaire.
Myriade, qui fonctionne pour le moment comme une unité de Quattrocento, développe des prototypes de l’instrument qui seront testés chez quatre partenaires (deux laboratoires et deux entreprises). Au programme : la mesure de concentration de virus pour l’immunothérapie, la mesure de concentration de bactériophages pour la phagothérapie, la mesure de phages dans le microbiote pour le diagnostic médical et la mesure de vésicules extracellulaires. Cette phase de tests devrait déboucher sur l’embauche d’une équipe propre à Myriade (directeur général, équipe R&D et équipe marketing et ventes) et sur la mise sur le marché du produit au premier trimestre 2019 à destination des laboratoires de biologie, de diagnostic médical et du domaine de l’environnement.
 |
Egalement dans Spectra Biologie n° 234 |
-
-
-
BOURSE & BIOTECHS
Un rapprochement phare et le retour de la thérapie génique
Arsia AMIR-ASLANI -
BIODÉBAT
Diagnostic et prise en charge de l’Insuffisance Rénale Aiguë
Guillaume BELLIARD, Christophe RENAUD, François SCHMITT -
MANIFESTATION
-
QUALITÉ
Dosage de la ciclosporine, du tacrolimus, de l’évérolimus et du sirolimus en LC-MS/MS
Isabelle PETIT, Anne BEZOL, Sybille GHACHAM, Karine CLAVAUD, Sabine HAVREZ,
Cécile MOUSSA, Carole EMILE, Pascal GERRIER - CAS BIOCLINIQUE
Une soupe « aux choux » empoisonnée
Yann BARGUIL, Natacha TATOYAN, Cyril ANTHEAUME, Marc MIKULSKI,
Elise CALTOT, Laurenco XAVIER
-
-
La Newsletter Spectra Biologie est une publication des Editions PCI
176, rue du Temple – 75003 Paris
Tél. : 01 44 59 38 38
www.spectrabiologie.fr – pci@pcipresse.com